- Inicio
- Signos y síntomas
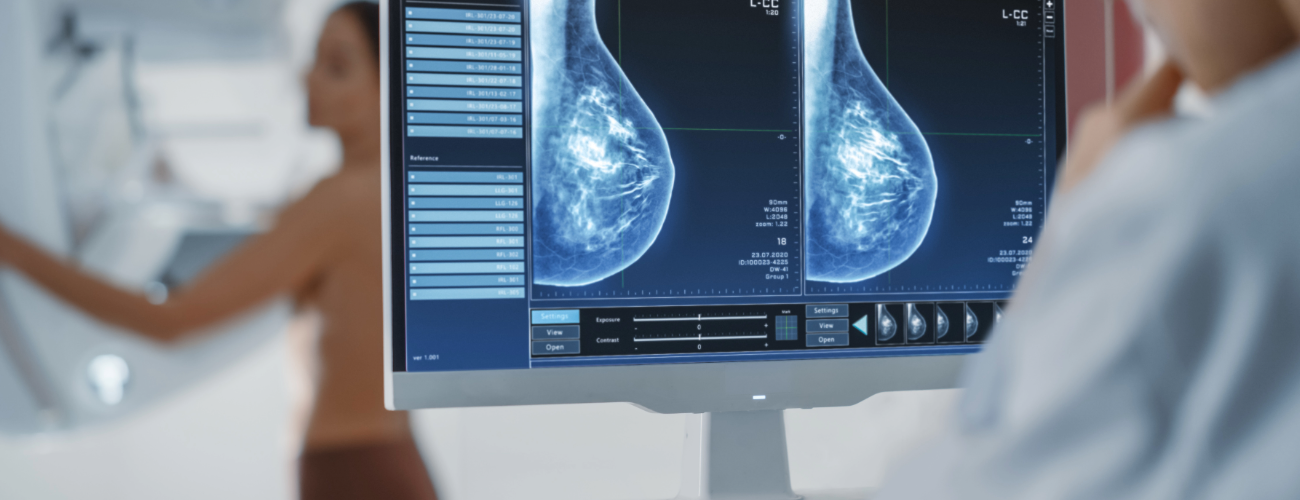
El beneficio de ladetección temprana
El diagnóstico precoz del cáncer de mama es vital para tratarlo de manera eficaz. Por ello es que los controles de rutina son determinantes y útiles para preservar la salud y bienestar.
Este material es de carácter educativo e informativo únicamente, no sustituye ni reemplaza la consulta médica, y en ningún caso deberá tomarse como consejo, tratamiento o indicación médica. Ante cualquier duda deberá consultar siempre con su médico tratante.
El cáncer de mama es el más frecuente en la mujer en el mundo: una de cada ocho mujeres podría desarrollar cáncer de mama durante algún momento de su vida.
La posibilidad de tratar con éxito esta enfermedad está asociada a varios factores, uno de ellos es el diagnóstico precoz: cuanto más temprano se diagnostique, mayor será la posibilidad de curación.
La detección temprana significa encontrar signos de la enfermedad antes de que aparezcan los síntomas. Hay distintas herramientas de diagnóstico por imágenes disponibles como:
- Mamografía: es el principal método utilizado para la detección de cáncer de mama ya que puede detectar lesiones malignas desde un año y medio hasta cuatro años antes de que una lesión sea clínicamente evidente. Sin embargo, un 15% de cánceres pueden pasar inadvertidos.
- Ecografía mamaria: es complementaria a la mamografía y se utiliza para la evaluación de lesiones sólidas o quísticas que no pueden ser evaluadas mediante la mamografía. Se usa especialmente en mujeres premenopáusicas porque el tejido mamario es más denso.
- Resonancia Nuclear Magnética: no es un estudio de rutina en el diagnóstico temprano y se reserva para mujeres con alto riesgo genético (portadoras de mutación genética).
¿Y el autoexamen?
El autoexamen mamario es una técnica muy difundida para la detección del cáncer de mama, sin embargo, está comprobado que esta técnica no tiene un efecto beneficioso para la salud de las mujeres que lo practican. Por un lado, genera falsas alarmas relacionadas con los cambios hormonales de las mamas durante el ciclo menstrual. Por otro, el autoexamen no es capaz de detectar nódulos tan pequeños como los que encuentra la mamografía.
De todas formas, el autoexamen cumple un rol de concientización en la mujer respecto a la anatomía y la salud de sus mamas. Es importante enfatizar que esta técnica no reemplaza a la mamografía. Cuando un tumor es palpable a través del autoexamen significa que ese tumor ya no está en una etapa primaria, pese a que sea sólo un bulto pequeño. Por ello, los especialistas enfatizan sobre la importancia de los métodos de diagnósticos por imágenes.
Si bien las recomendaciones médicas son genéricas, es importante indicar que no todas las mujeres presentan el mismo riesgo de desarrollar cáncer de mama y es primordial estimar cuál es ese riesgo para que, de esa manera, el médico especialista pueda recomendar la modalidad y la frecuencia del control mamario.
La mamografía se debe hacer dependiendo del grupo de riesgo de la mujer. Las mujeres sin antecedentes familiares de cáncer, deberían realizarse una mamografía anual a partir de los 40 años, mientras que, si efectivamente tienen antecedentes (madre, hermanas o tías que padecieron la enfermedad), el control mamográfico debería empezar diez años antes de la edad de diagnóstico del familiar que tuvo cáncer.
Por otro lado, si existiera algún pariente con cáncer, que además presentara una mutación genética (BRCA1 / BRCA2), entonces los controles deberían comenzar a los 30 años e incluso consultar si podría ser necesario realizar un estudio genético para saber si el paciente ha heredado esa mutación.
Los genes BRCA1 y BRCA2 generan proteínas que ayudan a reparar el ADN dañado de la célula. Cuando cualquiera de estos genes tiene una mutación, o alteración, por lo que no funcionan correctamente, el daño al ADN no puede repararse y la célula tiene más posibilidades de presentar alteraciones genéticas adicionales que pueden resultar en cáncer.
El estado del cáncer de mama
Una vez que se tiene la certeza de que existe un tumor maligno en la mama a través del diagnóstico por imágenes y del examen médico, se puede seguir con otro paso: la biopsia, que sirve para conocer el estado del cáncer de mama con mayor profundidad.
A grandes rasgos hay varios tipos de biopsias:
- Por punción con aguja gruesa (Tru-cut): a través de una aguja se extraen fragmentos de tejido mamario del área sospechosa.
- Excisional quirúrgica: esta técnica se realiza cuando se encuentra un nódulo palpable.
- Radioquirúrgica (BRQ): se utiliza para diagnosticar tumores que se presentan sólo con microcalcificaciones en la mamografía y sin lesión palpable.
Con la biopsia, se determina el estadio de la enfermedad considerando lo siguiente:
Criterios clínicos (TNM)
- El tamaño del tumor (T)
- Compromiso ganglionar axilar (N)
- Diseminación de la enfermedad a otros órganos (M)
Criterios anátomo patológicos:
- Grado histológico del tumor
- Presencia de Receptores Hormonales (Estrogénico y Progestínico)
- Expresión de la proteína HER2 en exceso
- Índice de proliferación (por IHQ) Ki 67
- Pruebas del perfil de expresión génica (Oncotype DX, MammaPrint, Prosigna)
Como conclusión, el médico tratante recopilará toda la información respecto al cáncer del paciente desde una variedad de fuentes que incluye:
- Examen físico.
- Informe de patología.
- Determinación del Subtipo intrínseco de cáncer de mama por determinación de Receptores Hormonales (Her2, Ki 67 Luminal A, Luminal B, Her2 y Basal o Triple Negativo por inmunohistoquímica).
- Imágenes de la mama. La mamografía, la ecografía y la resonancia magnética.
- Pruebas de imágenes adicionales en búsqueda de enfermedad metastásica.
Con esta información, médico y paciente podrán hablar sobre la estrategia de tratamientos más adecuada para el cáncer de mama.
1.Nyström L, Wall S, Rutqvist L, et al. Breast cancer screening with mammography: overview of Swedish randomised trials. The Lancet. 341, 1993: 973-978
2.Utzon-Frank N, Vejborg I, Euler-Chelpin E, et al Balancing sensitivity and specificity: Sixteen year's of experience from the mammography screening programme in Copenhagen, Denmark. Cancer Epidemiology. 35, Issue 5, October 2011, Pages 393-398
3.Thomas B D, Gao D, Ray R M, et al Randomized Trial of Breast Self-Examination in Shanghai: Final Results J Natl Cancer Inst 2002; 94:1445-1457.
4.S A Feig, et al. Digital Mammography. Radiographics Jul-Aug 1998;18(4):893-901
5.Humphrey L, Halfand M , Chan B, et al. Breast Cancer Screening: A Summary of the Evidence for the U.S. Preventive Services Task Force. Ann Intern Med. 2002 Sep 3;137(5 Part 1):347-60
6.Pisano ED, et al. Current Status of Full-Field Digital Mammography. Acad Radiol. 2000 Apr;7(4):266-80
7.Pisano ED, Digital Compared With Screen-Film Mammography: Measures of Diagnostic Accuracy Among Women Screened in the Ontario Breast Screening Program--Evidence That Direct Radiography Is Superior to Computed Radiography for Cancer Detection. Radiology 2016 Feb;278(2):311-2
8.Warner E, Messersmith H, Causer P, et al. Systematic Review: Using Magnetic Resonance Imaging to Screen Women at High Risk for Breast Cancer. Ann Intern Med 2008 May 6;148(9):671-9.
9.Lord SJ, Lei W, Craft P, et al. A Systematic Review of the Effectiveness of Magnetic Resonance Imaging (MRI) as an Addition to Mammography and Ultrasound in Screening Young Women at High Risk of Breast Cancer. Eur J Cancer 2007 Sep;43(13):1905-17.
10.Howlader N, Noone AM, Krapcho M, et al. (eds). SEER Cancer Statistics Review, 1975-2014, National Cancer Institute. Bethesda, MD, https://seer.cancer.gov/csr/1975\\_2014/, based on November 2016 SEER data submission, posted to the SEER web site, April 2017
11.Neal W Wilkinson , Azin Shahryarinejad, Janet S Winston. Concordance With Breast Cancer Pathology Reporting Practice Guidelines. J Am Coll Surg 2003 Jan;196(1):38-43
12.F Puglisi, A Follador, A M Minisini, et al. Baseline Staging Tests After a New Diagnosis of Breast Cancer: Further Evidence of Their Limited Indications Ann Oncol 2005 Feb;16(2):263-6.
13.Alberto Ravaioli, Giuseppe Pasini, Antonio Polselli,Staging of Breast Cancer: New Recommended Standard Procedure. Breast Cancer Res Treat. 2002 Mar;72(1):53-60.
14.A Arnaout, N P Varela, M Allarakhia, et al. Baseline Staging Imaging for Distant Metastasis in Women With Stages I, II, and III Breast Cancer Curr Oncol. 2020 Apr;27(2):e123-e145.
15. Kuchenbaecker KB, Hopper JL, Barnes DR, et al. Risks of breast, ovarian, and contralateral breast cancer for BRCA1 and BRCA2 mutation carriers. JAMA 2017; 317(23):2402-2416.
16.Brose MS, Rebbeck TR, Calzone KA, et al. Cancer risk estimates for BRCA1 mutation carriers identified in a risk evaluation program. Journal of the National Cancer Institute 2002; 94(18):1365–13
17.Levy-Lahad E, Friedman E. Cancer risks among BRCA1 and BRCA2 mutation carriers. British Journal of Cancer 2007; 96(1):11–15
18.U.S. Preventive Services Task Force. Risk Assessment, Genetic Counseling, and Genetic Testing for BRCA-Related Cancer in Women: Clinical Summary of USPSTF Recommendation. AHRQ Publication No. 12-05164-EF-3. December 2013 http://www.uspreventiveservicestaskforce.org/uspstf12/brcatest/brcatestsumm.htm
19.Burke W, Daly M, Garber J, et al. Recommendations for follow-up care of individuals with an inherited predisposition to cancer. II. BRCA1 and BRCA2. Cancer Genetics Studies Consortium. JAMA 1997; 277(12):997–1003.
PP-UNP-ARG-1706